La calculadora para La Arrhenius Energía de Activación para Dos Temperaturas usa La Ecuación de Arrhenius para computa la energía de activación basarse en dos temperaturas y dos constantes de la velocidad de reacción.
INSTRUCCIONES: Elija las unidades e introduzca lo siguiente:
- (k1) representa el constante de la velocidad de reacción
- (k2) representa el constante de la velocidad de reacción
- (T1) representa la primera temperatura
- (T2) representa la segunda temperatura
Energía de Activación: La calculadora devuelve la energía de activación en Julios por mol.
La Lógica
La Ecuación de Arrhenius, `k = A*e^(-E_a/"RT")`, lo puedes reescribe (como se muestra abajo) para muestrar el cambio de k1 a k2 cuando hay un cambio en la temperatura T1 to T2. Se usa esta ecuación para calcular la energía de activación de una reacción cuando hay múltiple temperaturas. Los entradas son las siguientes:
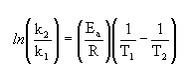
· k1 representa el constante de la velocidad de reacción en la primera temperatura
· k2 representa el constante de la velocidad de reacción en la segunda temperatura
· Ea representa la energía de activación en Julios por mol (J/mol)
· R representa el constante de gas ideal (8.314 J/mol*K)
· T1 representa la primera temperatura en Kelvin (K)
· T2 representa la segunda temperatura en Kelvin (K)
La calculadora converta los dos temperaturas en Kelvin para que puedan cancelar.
Más Información
ChemistNate: Example of Arrhenius Equation
Khan Academy: Using the Arrhenius Equation
Referencias Bibliográficas
Whitten, et al. "Chemistry" 10th Edition. Pp. 645